华辰生物七款核心产品获FDA DMF备案,全链条赋能CGT国际化

苏州华辰生物科技有限公司自主研发的七款核心产品已先后获得美国食品药品监督管理局(FDA)药物主文件(DMF)备案,覆盖细胞培养、扩增、冻存及规模化生产全流程,为国内CGT企业开展中美双报及国际化申报提供系统化的原料支持。
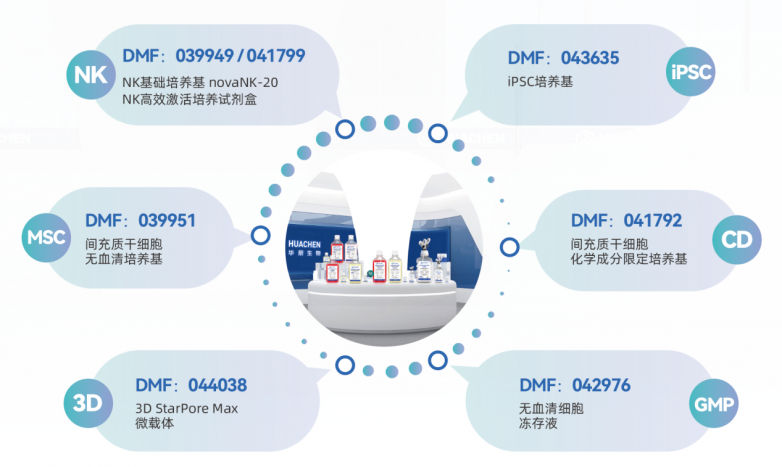
一、七款备案产品及DMF号
1、novaNK-20 NK细胞无血清培养基(DMF 039949)
专为NK细胞培养开发
化学成分限定
和市场上同类产品相比,细胞增殖更快,细胞活率更高,细胞密度更高
培养袋培养细胞密度可达4-5E6/ml
含重组人胰岛素、重组人血白蛋白
所有nova系列培养基药物主文件已提交至FDA,获得DMF备案号
GMP level,内毒素低于0.1EU/ml
2、NK高效激活培养试剂盒(DMF 041799)
高倍数:day28>10万倍
高数量:day21天1000-1500亿
高纯度:高效版CD3-CD56+>98%;增强版CD3-CD56+>90%;CD16+CD56+>90%
高活率:细胞活率>90%
低成本:每份NK制剂生产成本是原来的1/3-1/5
异体用:CD3+细胞<1%,满足异体使用
纯因子:feeder free,GMP 生产,DMF备案
3、间充质干细胞无血清培养基(DMF 039951)
适用于原代细胞分离及传代培养
兼容多种间充质干细胞,脐带、脂肪、骨髓、羊膜、毛囊、牙髓等
无血清,无任何动物源组分,不含抗生素,性能稳定,批间差异小
高细胞扩增率,单个代次扩增倍数达20倍以上
单个T175收获细胞>2E7,单个十层细胞工厂收获8-10亿
细胞直径14-15μm,小于市场同类型产品
GMP level,注射用水配制,内毒素<0.1EU/ml
自主化研发与生产体系,供货稳定,性价比高
适配3D微载体培养,已完成10L/50L工艺开发
4、间充质干细胞化学成分限定培养基(DMF 041792)
无血清,不含血小板裂解物
无动物源成分
无人源成分,含重组人血白蛋白
化学成分明确,批间高度一致性
高效性,支持MSCs原代和传代培养
GMP规范生产,支持药物申报
更高质量,内毒素<0.1EU/ml
5、3D StarPore® Max微载体(DMF 044038)
药辅级明胶成分柔性多孔设计
辐照灭菌,封闭管道,免费看片+app即开即用
颗粒圆整,大小均一,无碎片
支持更高密度接种,单位载体更高产量
细胞直径小于同类产品
一级罐10L 百亿,二级罐50L 500亿,载体用量更省
专用裂解液20分钟内温和消化
更大的比表面积,更高的扩增倍数
支持种子细胞含DMSO直接接种
6、无血清细胞冻存液(DMF 042976)
无血清
化学成分明确无动物源成分
临床注射级成分即用型
-80℃与-196℃兼容 cGMP制造
7、iPSC培养基(DMF 043635)
适用于人诱导多能干细胞和胚胎干细胞
无血清,无任何动物源组分,不含抗生素,安全可靠
长期高效扩增,支持连续稳定扩增20代以上
增强缓冲系统 ,支持隔天换液
可用于 iPSC 3D大规模扩增,性能稳定
化学成分限定,含重组人血白蛋白
上述产品协同覆盖了CGT上游的核心环节:
细胞培养:iPSC培养基、MSC无血清/化学成分限定培养基、novaNK-20培养基
功能激活:NK高效激活培养试剂盒
规模化生产:3D StarPore® Max微载体(10L→百亿,50L→500亿)
细胞保存:无血清细胞冻存液
二、DMF备案价值:为客户出海搭建“合规快车道”
药物主文件(DMF)是美国FDA用于收录关键原料技术资料的系统。获得备案后,下游制药企业在进行新药临床试验(IND)或上市申请时可直接引用备案号,无需重复提交原料的详细工艺与质控数据,从而显著缩短审评周期、降低申报风险。
华辰生物七款产品集中备案,使客户在干细胞治疗、免疫细胞治疗等项目的国际申报中,能够同时获得培养基、试剂盒、微载体、冻存液等多个环节的合规支持,真正实现“一站式”溯源。

三、国产替代与国际化标准并行
长期以来,CGT上游高端原料市场被进口品牌垄断。华辰生物从原料(药用辅料级)、生产工艺(GMP)到质控体系(FDA DMF),完全实现自主研发与国产化生产。
本次七款产品获得FDA DMF备案,是华辰生物响应国家“国产替代”战略、推动中国CGT产业链迈向国际化标准的重要里程碑。公司已建成1000L培养基自动化生产线和2500平方米研发生产基地,持续为行业提供从科研级到GMP级别的可靠原料。
未来,华辰生物将继续深耕细胞治疗上游核心领域,拓展更多产品线的国际合规认证,携手产业链伙伴降低中国CGT企业的出海门槛,助力创新疗法惠及全球患者。
如需获取DMF授权信或产品技术资料,欢迎通过华辰生物官方渠道联系。


